Dacă o să căutați pe Internet ce este pH-ul, o să găsiți nenumărate articole. Din păcate, nu există niciunul (ori cel puțin nu am putut găsi unul) care să explice într-o manieră simplă, ușor de înțeles, fără cuvinte complicate, dar care să te lămurească pe deplin, mergând la nivel fundamental cu explicația. Acesta e scopul acestui articol!

O explicație care introduce concepte misterioase, fără a le explica pe înțelesul tuturor, obligă la memorare, dar în lipsa înțelegerii intervine uitarea în scurt timp.
Asta încercăm să facem în acest articol: să explicăm ce este pH-ul, pornind de la bază, adică de la molecula de apă. Vom discuta despre: ionizarea apei; ce înseamnă acid și bază; ce măsoară de fapt sistemul pH; cum reglează organismul pH-ul; care este pH-ul unor substanțe din viața de zi cu zi.
Molecula de apă
Molecula de apă este formată din doi atomi de hidrogen și un atom de oxigen. Un atom de hidrogen este format dintr-un proton, care formează nucleul, și un electron. Atomul de oxigen are, în schimb, 8 electroni (2 pe primul strat energetic, 6 pe ultimul strat).
Molecula de apă se formează în felul următor: atomul de oxigen pune în comun doi electroni din cei șase de pe ultimul strat, iar doi atomi de hidrogen își pun în comun singurul lor electron, ca în imaginea de mai jos.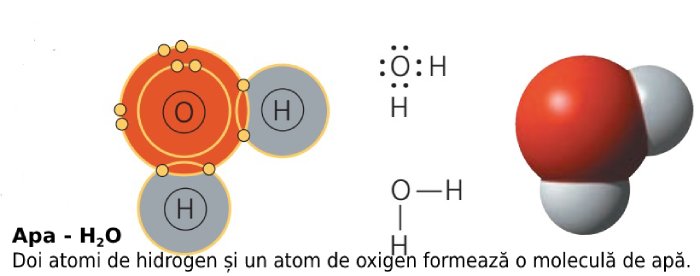
Apa formează ioni
Apa are capacitatea de a forma ioni în mod natural. Acest proces este relativ rar, însemnând că o moleculă din 554 de milioane de molecule se va ioniza.
Ce înseamnă că o moleculă de apă se ionizează? Înseamnă că, în mod natural, o moleculă de apă se va separa într-un ion pozitiv de hidrogen, H+ (rămâne, practic, un proton, căci asta rămâne dintr-un atom de hidrogen care își pierde electronul), și un ion hidroxid, OH-. Cu alte cuvinte, o moleculă de apă pierde un atom de hidrogen în favoarea unei alte molecule de apă (păstrând însă electronul atomului de hidrogen).
** Notația H+ arată că hidrogenul a pierdut un electron (semnul plus arată „pozitivitatea” ionului de hidrogen, căci electronul este negativ, iar elementul negativ, electronul, a dispărut).
** În schimb, notația OH- ne arată că acest compus chimic are o „negativitate” suplimentară (de aici „minusul”), pentru că a acumulat un electron de la atomul de hidrogen care a părăsit molecula de apă.
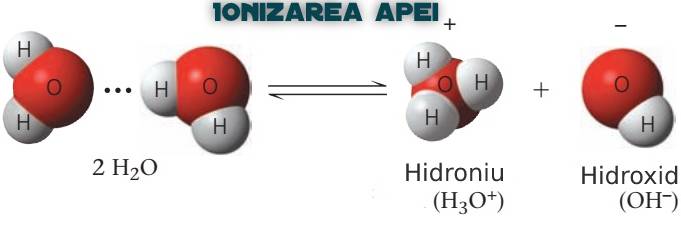
În realitate, protonul liber formează imediat o legătură cu o moleculă de apă (H2O), formând H3O+ (așa cum se vede în imaginea de mai sus). Deși în multe cărți se vorbește despre H+ și se sugerează ideea că protonii rămân izolați între moleculele de apă, în fapt aceștia, cum spuneam, se atașează unei molecule de apă, iar noul compus, ionul hidroniu (H3O+), este cel la care ne referim când menționăm ionul pozitiv de hidrogen, H+.
Prin urmare, în apa pură cantitățile de H3O+ și OH- sunt egale, din fiecare existând o concentrație de 1x10-7 mol/litru. Dacă e să numărăm ionii hidroniu dintr-un litru de apă, vom găsi peste 60.000 de trilioane. Mulți, dar puțini în comparație cu restul moleculelor de apă dintr-un litru.
Ce este molul?
Am menționat „molul” paragraful de mai sus, vorbind despre cantitatea de H3O+ și OH-. Ce este molul?
Un mol reprezintă un număr de unități dintr-o substanță chimică, iar unitățile pot fi atomi sau molecule. Numărul de unități care definesc un mol este cunoscut drept numărul lui Avogadro și are valoarea 6,02x1023.
Asta înseamnă că un mol de oxigen molecular (O2) va avea 6,02x1023 de astfel de molecule. Un mol de ion hidroniu va avea 6,02x1023 de astfel de ioni. Desigur, pentru că masa fiecărei unități (hidroniu, oxigen molecular șamd) este diferită, un mol de o substanță are masa diferită de un mol de altă substanță. Molul este identic în numărul de unități, nu în masa absolută.
Acizi și baze
Orice substanță care poate dona un proton se numește acid, iar una care acceptă un proton se numește bază.
Apa e și una, și alta, pentru că are, cum spuneam, aceeași cantitate de ion hidroniu (care poate ceda un proton) și de ion hidroxid (care poate primi un proton).
Acidul
Dar apa este neutră. Ce o poate transforma într-un acid? Un dezechilibru al concentrațiilor de ion hidroniu și de ion hidroxid. Cum se poate ajunge aici? Prin dizolvarea unui acid.
Un acid este o substanță care crește concentrația de ion hidroniu dintr-o soluție. De exemplu, acidul clorhidric (HCl). Atunci când este pus în apă, moleculele de acid clorhidric se separă în H+ (ion de hidrogen, adică un proton) și Cl- (un atom de clor cu un electron suplimentar, luat de la hidrogen).
HCl --> H+ + Cl-
În acest fel, prin acest adaos de H+, aciditatea apei crește, căci dispare echilibrul dintre ion hidroniu (care crește numeric) și ion hidroxid (care rămâne la fel numeric).
Baza
O substanță ce reduce concentrația de ion hidroniu se numește bază. Cum face baza asta? Prin acceptarea de ioni de hidrogen. Un exemplu de bază este amoniacul (NH3), care atrage ioni de hidrogen din apă, rezultând ion amoniu (NH4+).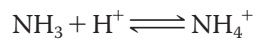
Săgețile în ambele sens din formula de mai sus arată că amoniacul este o bază slabă, legăturile cu ionii de hidrogen fiind instabile (se formează și se rup ușor).
Soluțiile cu o mai mare concentrație de ion hidroxid (OH-) sunt numite soluții bazice.
Sistemul pH de măsurare a acidității
Am învățat o serie de noțiuni importante până acum:
· am aflat că molecula de apă se ionizează (un atom de hidrogen dintr-o moleculă se rupe de aceasta, formând o legătură cu altă moleculă de apă), rezultând ion hidroniu și ion hidroxid, în cantități egale - ceea ce face ca apa pură să fie nici acid, nici bază, ci o soluție neutră;
· am aflat că există substanțe (numite acizi sau baze) care reacționează cu apa și schimbă acest echilibru dintre H3O+ și OH-.
Înțelese aceste lucruri, putem vorbi despre pH, dat fiind că avem toate cunoștințele necesare.
Așadar, concentrația de ioni hidroniu (dar și de ion hidroxid) este de 1x10-7 mol/litru. 10-7 este baza pentru sistemul pH care măsoară aciditatea unei soluții. pH se referă la protonii de hidrogen.
Logaritmul negativ al lui 10-7 este 7, așa că o soluție neutră va avea pH-ul 7.
Atunci când concentrația de H+ (ne referim la ionul hidroniu) crește la 10-6 mol/kg, pH-ul este 6 șamd.
Cum a apărut termenul „pH”?
Termenul „pH” a fost folosit întâi de biochimistul Søren Peter Lauritz Sørensen în anul 1909.
pH, conform unor interpretări, este abrevierea expresiei: „puterea oxigenului”, „p” venind de la „potenz”, care înseamnă „putere” în germană, iar „H” venind de la hidrogen. Mai puteți găsi și interpretarea: „potențialul hidrogenului”.
Interesant este că autorul, biochimistul danez, nu a explicat nicăieri care este logica acestei abrevieri, pH.
J G Nørby, în articolul „The Origin and the Meaning of the Little P in pH”, încearcă să găsească explicația definitivă. Concluzia acestuia, din articolul menționat, este: „se pare că micul „p” din pH este o consecință a alegerii întâmplătoare a literelor p și q pentru a indica două soluții în explicația sa inițială a metodei electrometrice”.
Mai e interesant de știu că Sørensen a folosit varianta PH, nu pH (puteți vedea aici detalii); cum s-a ajuns la varianta actuală, cu p-ul mic, este un mister.
Produsul dintre H+ și OH- este constant
În orice soluție apoasă la 25° C produsul dintre H+ și OH- este mereu 10-14.
[H+][OH-]=10-14
Dacă se adaugă suficient acid unui substanțe, crescând concentrația de ion hidroniu la 10-6, concentrația de ion hidroxid va coborî la 10-8 (produsul dintre cele două menținându-se constant, 10-14). Cum e posibil? Un acid nu doar adaugă ioni unei soluții, ci, de asemenea, elimină ioni hidroxid (ca urmare a formării de legături dintre H+ și OH-, formând, prin urmare, molecule de apă).
pH-ul și sănătatea
pH-ul este foarte important pentru sănătatea unui organism. De exemplu, pH-ul sângelui trebuie să stea între 7,35 și 7,45. Valori sub 6,8 și peste 7,45 pot duce la distrugerea legăturilor din proteine, putând surveni decesul. Dar există mecanisme interne care reglează pH-ul organismului ori de câte ori este nevoie.
Schimbă alimentația pH-ul din corpul uman?
Dietele care spun că schimbă pH-ul mint. Organismul are propriul mecanism de păstrare a pH-ului în limitele acceptabile. Dar dacă cei care clamează schimbarea pH-ului prin nu știu ce alimente minune ar avea dreptate, ar fi rău, căci ar fi în detrimentul sănătății. pH-ul trebuie să stea constant, iar pentru asta organismul și-a creat instrumentele potrivite, așa cum puteți vedea mai jos.
pH-ul a diverse substanțe
Iată câteva exemple de substanțe și pH-ul acestora:
· acidul de baterie: pH - 1 (asta înseamnă o concentrație masivă de ion hidroniu).
· sucul de lămâie și sucul gastric: pH - 2
· vinul, cola: pH - 3
· sucul de roșii: pH - 4
· saliva: pH - 6
· apa pură: pH - 7
· apa de mare: pH - 8
· amoniacul: pH - mai mare de 11
· soluția de curățat aragazul: pH - mai mare de 13
În prima imagine a articolului puteți vedea pH-ul mai multor substanțe.
Cum reglează organismul uman pH-ul?
Cum spuneam, sângele uman are un pH un pic mai mare decât 7, fiind așadar ușor bazic. Păstrarea pH-ului între anumite limite (7,35 și 7,45) este esențială; ieșirea din aceste limite poate duce la moartea rapidă a organismului.
Dacă adăugăm 0,01 mol de acid puternic într-un litru de apă pură, pH-ul scade de la 7 la 2.
Dar dacă adăugăm aceeași cantitate de acid unui litru de sânge, pH-ul sângelui va coborî de la 7,4 la 7,3. Cum e posibil așa ceva?
Organismul dispune de anumite substanțe, soluții tampon, care au capacitatea de a minimiza rapid schimbările concentrației de ion hidroniu sau ion hidroxid. Cum fac aceste substanțe asta? Cunoașteți deja „rețeta”: prin „donarea” ori acceptarea de ioni de hidrogen. Un exemplu de soluție tampon este acidul carbonic (H2CO3), care se formează atunci când dioxidul de carbon (CO2) intră în reacție cu apa din plasma sanguină. Acidul carbonic are capacitatea de a regla pH-ul în ambele „direcții”, eliminând ori adăugând ioni de hidrogen sângelui.
Sumar
Ok, a fost un drum lung. Iată principalele idei ale acestui articol:
· pH-ul unei substanțe arată echilibrul dintre concentrația de ion hidroniu și concentrația de ion hidroxid;
· acizii și bazele sunt acele substanțe care au capacitatea de strica acest dezechilibru, într-o direcție sau alta;
· pH-ul organismului este reglat intern, prin intermediul unui mecanism ce utilizează anumite substanțe chimice.
Informațiile, în bună parte, sunt din cartea Biology, ed. a 10-a, editura Pearson.
