
În acest articol vom vorbi despre ce se întâmplă, la nivel atomic, atunci când punem o lingură de sare într-o cană cu apă. Vom explica de ce molecula de sare se dizolvă în apă, pe înțelesul tuturor, fără a fi nevoie de cunoștințe de chimie sau fizică. Pentru a înțelege ce se întâmplă cu sarea, trebuie să înțelegeți, întâi, ce e așa special cu apa: cum se formează, care sunt proprietățile care o transformă într-un solvent.
Atomii sunt formați din nucleu și electroni. Nucleul atomilor este format din protoni și neutroni, particule care nu sunt elementare, ci sunt formate din quarcuri, care sunt particule elementare. În acest articol ne focalizăm pe electroni, particule cu sarcină negativă, așezate în straturi energetice în jurul nucleului.
Legăturile chimice implică întotdeauna electroni, în special electronii de pe ultimul strat energetic. Numărul și tipul de legături chimice pe care le pot stabili atomii depinde de numărul de electroni pe care atomii îi pot pune în comun, ceda sau primi.
Legăturile chimice care presupun punerea în comun de electroni se numesc legături covalente. Mai sunt și alte tipuri de legături, dar nu ne interesează în articolul de față.
→ Citiți și: Cum funcționează legăturile chimice
Molecula de apă
Molecula de apă este formată din doi atomi de hidrogen și un atom de oxigen. Un atom de hidrogen este format dintr-un proton, care formează nucleul, și un electron. Atomul de oxigen are, în schimb, 8 electroni (2 pe primul strat energetic, 6 pe ultimul strat).
Molecula de apă se formează în felul următor: atomul de oxigen pune în comun doi electroni din cei șase de pe ultimul strat, iar doi atomi de hidrogen își pun în comun singurul lor electron, ca în imaginea de mai jos.
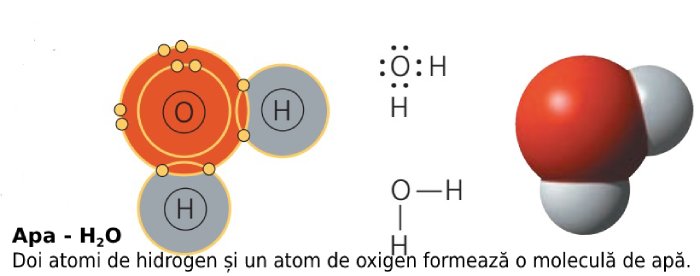
Electronegativitatea apei
Electronegativitatea se referă la capacitatea nucleului atomic de a păstra electronii de pe stratul energetic cel mai îndepărtat. Unii atomi, ca cei de oxigen, au electronegativitate mare, ceea ce înseamnă, metaforic vorbind, că „țin cu dinții” de electronii lor, pe când alți atomi, ca sodiul, au electronegativitatea foarte scăzută, adică renunță ușor la electronii de pe ultimul strat energetic.
Ce legătură are electronegativitatea cu apa?
Oxigenul are o electronegativitate mare în comparație cu atomul de hidrogen. Asta înseamnă că electronii puși în comun de atomii de oxigen și hidrogen sunt mai aproape (un fel de a spune...) de nucleul atomului de oxigen, oxigenul obținând în felul ăsta o sarcină negativă parțială (δ‾), iar hidrogenul o sarcină parțială pozitivă (δ+).
Așadar, pentru că electronii sunt mai aproape de nucleul oxigenului, iar electronii au sarcini negative, atomii de oxigen devin mai negativi. Apare o distribuție neuniformă a sarcinii în molecula de apă, care îi dă acesteia proprietățile foarte interesante pe care le are.
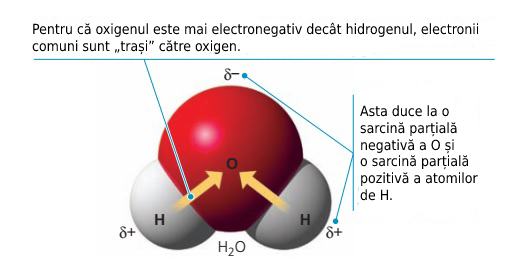
Legătură polară
Spuneam că legătura chimică între atomii care pun în comun electroni se numește legătură covalentă. Când avem doi atomi cu electronegativitate diferită, cum e cazul oxigenului și hidrogenului, atunci numim legătura polară. Așadar, o moleculă de apă este polară, referindu-se tocmai la distribuția inegală a sarcinii explicată mai sus.
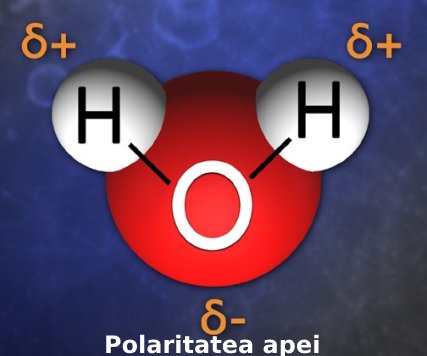
Legătura de hidrogen
Sarcinile parțiale pozitive ale hidrogenului sunt atrase de sarcinile parțiale negative ale oxigenului, căci sarcinile opuse se atrag. Acest tip de legătură se numește legătura de hidrogen.
Legătura de hidrogen nu se referă la legătura covalentă dintre atomii de hidrogen și oxigen care formează o moleculă de apă, ci la legătura care se formează între atomii de hidrogen ai unei molecule de apă și atomii de oxigen ai altei molecule de apă (vezi imaginea de mai jos).
Legăturile de hidrogen reprezintă motivul pentru care apa rămâne lichidă la temperatura camerei. Aceste legături se desfac ușor, nu sunt permanente, fiecare moleculă de apă formând și încetând aceste legături continuu cu moleculele de apă din jur. Este ceea ce dă apei caracterul fluid, maleabilitatea, capacitatea de a lua forma oricărui vas.
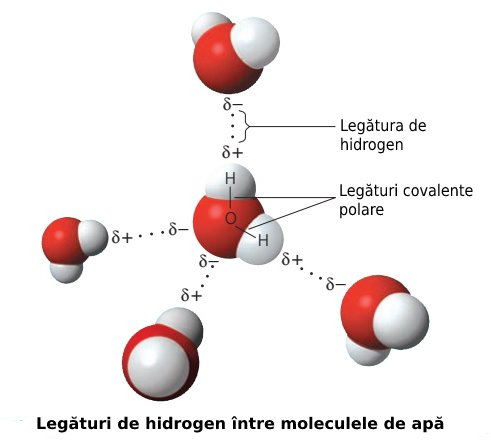
Un caz aparte este atunci când temperatura scade sub zero grade Celsius. Citiți aici ce se întâmplă cu apa: De ce gheața plutește
Apa este un solvent
Ce înseamnă că este un solvent? Adică are capacitatea de a dizolva diverși compuși. Și ne apropiem de momentul în care explicăm cum se dizolvă sarea în apă.
Cum se formează sarea?
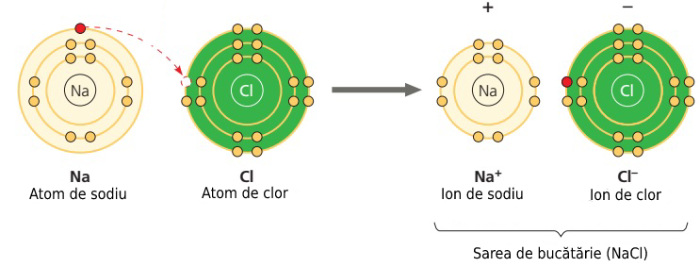
Sarea de bucătărie este un compus chimic care se formează dintr-un atom de clor și un atom de sodiu. Sodiul are 11 electroni, 2 în primul strat energetic, 8 în al doilea și 1 în ultimul. Clorul are 17 electroni, 2 în primul strat, 8 în al doilea, 7 în ultimul (vezi imaginea de mai jos).
Atunci când un atom de sodiu se întâlnește cu un atom de clor, un electron de la atomul de sodiu va fi „furat” de atomul de clor, care-și va completa ultimul strat energetic. Produsul format este sarea de bucătărie.
Gândiți-vă la următorul lucru: sodiul (Na), în stare pură, e un metal. Clorul (Cl), în stare pură, e un gaz otrăvitor. Când iei atomul de clor și-l pui lângă cel de sodiu, iese sarea de bucătărie (NaCl), nici metal, nici otrăvitoare. Acesta e un exemplu de emergență: produs cu trăsături diferite de cele ale componentelor.
Atunci când un atom pierde ori primește electroni, se numește ion (pozitiv sau negativ, dacă cedează ori primește). Sarea este un compus format, așadar, din doi ioni, unul de sodiu (+), care a cedat un electron, și unul de clor (-), care a primit un electron.
Cum se dizolvă sarea în apă
În fine, am ajuns la momentul adevărului! Știm acum ce este electronegativitatea, înțelegem, deci, că molecula de apă are o sarcină distribuită inegal, știm ce este legătura de hidrogen, care permite ca moleculele de apă să se „cupleze” între ele, știm ce este un ion. Avem tot bagajul de cunoștințe pentru a explica cum se dizolvă sarea în apă.
Când spunem că sarea se dizolvă în apă, în fapt spunem că sarea se transformă în ioni de sodiu și clor. Iată cum se întâmplă acest lucru.
Ionul de clor, care este un ion negativ (a primit un electron de la sodiu) formează legături cu atomii de hidrogen din moleculele de apă din jur. Legătura sa cu ionul de sodiu este mai slabă decât legătura care se formează cu atomul de hidrogen, așa că legătura strânsă în condiții de lipsă a apei se duce pe apa sâmbetei.
În același timp ionul de sodiu (ion pozitiv, căci a cedat un electron clorului) va forma legături cu atomii de oxigen.
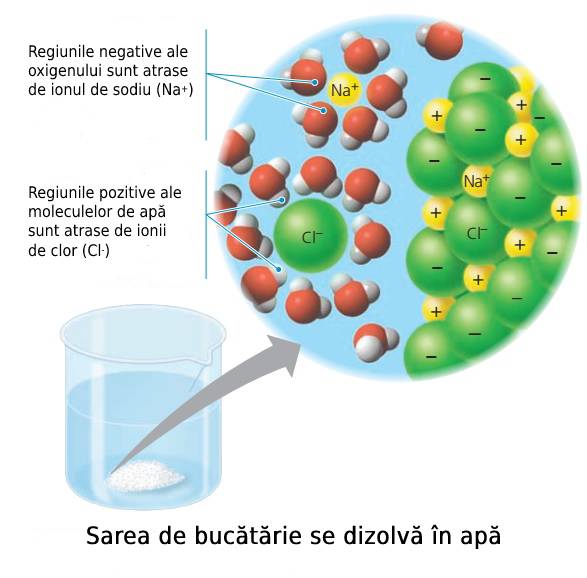
Altfel spus, odată ajunși în apă, ionii care formează sarea de bucătărie stabilesc legături noi cu atomii care formează moleculele de apă. Asta explică misterul dizolvării sării în apă!
Imaginile sunt preluate din cartea Campbel Biology, ediția a 10-a, și adaptate în lb. română.
