
Atomul de hidrogen (reprezentare grafică), format dintr-un proton şi un electron
Numărul atomic, notat cu litera Z, indică numărul de protoni (particule cu sarcină electrică pozitivă) din interiorul nucleului unui atom. Numărul atomic este cea mai importantă caracteristică a unui atom, pentru că numărul de protoni dă identitatea unui element chimic. De exemplu, atomul de hidrogen, cel mai simplu atom, are un singur proton. Un atom care are doi protoni se numește heliu. Dacă are trei protoni, vorbim de atomul de litiu, iar dacă are șase, vorbim de carbon.
Pe scurt, un atom este format din electroni (particule elementare care au sarcină negativă), situați în straturi energetice la exteriorul atomului, și nucleu. Nucleul este format, în principiu, din protoni și neutroni. În principiu, pentru că ați văzut că atomul de hidrogen are un proton și niciun neutron.
Dar protonii și neutronii nu sunt particule elementare (care nu pot fi descompuse în alte particule), ci sunt formate din alte particule denumite quarcuri. Formal, protonii sunt alcătuiți din trei quarcuri, care sunt ținuți împreună de particule-mesager fără masă numite gluoni, dar realitatea este mai complicată.
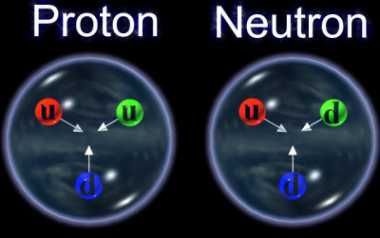
Un proton este alcătuit din quarcuri de două tipuri (două quarcuri up și un quarc down). Ca în imaginea de mai jos.
Pentru ca un atom să fie neutru din punct de vedere electric, trebuie să fie într-o stare de echilibru în ce privește numărul de protoni (+) și numărul de electroni (-), adică numărul de protoni să fie egal cu numărul de electroni. Asta pentru că sarcina unui electron este egală și de semn opus cu sarcina unui proton.
Pentru că numărul de protoni dictează numărul de electroni, în esență numărul de protoni determină proprietățile chimice ale unui atom.
→ Citește și: Cum funcționează legăturile chimice
În interiorul unui atom poate varia numărul de neutroni, particulă fără sarcină electrică. Atomii de același tip (același număr de protoni), dar cu număr diferiți de neutroni se numesc izotopi. Puteți citi mai multe despre izotopi aici.
→ Citește mai multe despre atom aici: Modelul cuantic al atomului
