 Dacă Universul ar fi o prăjitură, cum l-aţi putea crea? Care este reţeta după care acesta a fost construit? Care sunt ingredientele de bază necesare? Pentru ca înţelegerea să fie deplină, vom face o scurtă trecere în revistă a descoperirilor importante privind ingredientele fundamentale.
Dacă Universul ar fi o prăjitură, cum l-aţi putea crea? Care este reţeta după care acesta a fost construit? Care sunt ingredientele de bază necesare? Pentru ca înţelegerea să fie deplină, vom face o scurtă trecere în revistă a descoperirilor importante privind ingredientele fundamentale.
În această serie de articole vom trece în revistă cum au răspuns oamenii de ştiinţă la această întrebare de-a lungul timpului ajungând până în ziua de astăzi, când la Geneva a fost lansat recent cel mai complex instrument ştiinţific construit vreodată, acceleratorul Large Hadron Collider, tocmai pentru a perfecţiona răspunsul nostru la întrebările: care este reţeta şi care sunt ingredientele elementare ale Universului?
Universul: reţetă şi ingrediente, partea I
Povestea noastră începe în Grecia Antică, acum cam 2500 de ani (circa 500 î.Hr.). Atunci s-au creat primele şcoli în care oamenii priveau atent în jur, observau o diversitate mare de animale, de plante, de substanţe şi se întrebau din ce sunt toate acestea formate şi cum au fost ele create. Altfel spus, care sunt ingredientele şi care sunt legile, reţeta, după care sunt create obiectele din jurul nostru, ba chiar din Universul întreg. Şi cele mai înţelepte minţi ale vremii au găsit un răspuns care i-a mulţumit: totul ar fi creat din patru elemente fundamentale - apă, aer, pământ şi foc. În variate combinaţii, acestea dădeau toată diversitatea din jurul nostru. Ingredientele Universului propuse erau clare, dar reţeta după care acestea erau combinate în substanţele din viaţa de zi cu zi rămânea un mister. Iată aşadar prima încercare de a defini ingredientele şi reţeta Naturii. Oamenii care şi-au pus întrebările şi au dat aceste răspunsuri erau numiţi filosofi.
Timpul a trecut, secole după secole, iar strădania de a cunoaşte lumea din jurul nostru a continuat. Pe lângă filosofi au apărut filosofi ai naturii, alchimişti şi astrologi. Filosofii naturii studiau fenomenele din viaţa de zi cu zi; alchimiştii studiau substanţele şi încercau să le schimbe proporţia de apă, aer, pământ şi foc pentru a putea produce metale scumpe, precum aurul, sau un elixir al vieţii veşnice; astrologii studiau mişcarea planetelor pe cer cu scopul de a determina viitorul. Astfel era situaţia în Evul Mediu, acum cam 500 de ani (circa anul 1500).
Timpul a trecut şi uşor-uşor filosofii naturii au devenit fizicieni, alchimiştii au devenit chimişti, iar astrologii astronomi. Şi ştiinţa adevărată a luat viaţă, adică aceea care propune un răspuns matematic pe care apoi îl testează experimental. Experimentul este judecătorul suprem al unei teorii ştiinţifice.
Şi iată că acum doar 250 de ani (circa 1750), au avut loc primele semne că ingredientele Universului nu ar fi cele patru considerate în Antichitate. Chimiştii au arătat atunci că există substanţe care nu sunt create la rândul lor din alte substanţe. Erau substanţe elementare, sau elemente. Mai mult, cele pe care le credeau elemente erau de fapt substanţe compuse: apa era formată din oxigen şi hidrogen, aerul din oxigen şi azot, pământul era format din diferite alte substanţe sfărâmate, iar focul... focul era încă un mister, dar măcar se ştia că focul nu poate exista fără oxigen şi că arderea este compunerea unei substanţe chimice cu oxigenul.
Iată, aşadar, cum după mai bine de 2250 de ani, civilizaţia vestică descoperea că de fapt ingredientele Universului sunt o serie de câteva zeci de elemente chimice, iar nu cele patru elemente din Antichitate. Dar care era reţeta după care acestea erau combinate în substanţe compuse era încă necunoscut. Despre aceasta, în ediţia viitoare.
Universul: reţetă şi ingrediente, partea a II-a
Am văzut mai sus cum în Antichitate (circa 500 î. Hr.) se credea că ingredientele fundamentale ale Universului ar fi patru elemente (apă, aer, pământ şi foc) care se combinau după legi necunoscute pentru a crea toate substanţele din jur, inclusiv organismele vii. Şi am văzut cum ştiinţa modernă credea, în jur de anul 1800, că ingredientele fundamentale ale Universului ar fi de fapt câteva zeci de elemente chimice, care se combină tot după legi încă necunoscute. În acest articol vom continua aventura în lumea ingredientelor şi reţetei Universului.
Următoarea schimbare de paradigmă (adică a modului în care omenirea înţelege Universul) a avut loc exact acum 200 de ani, când chimistul britanic John Dalton a descoperit... atomii. Fiecărui element chimic îi corespundea câte un tip de atom, atomii se combinau după legi încă necunoscute pentru a crea diverse tipuri de molecule, iar moleculele generau diversitatea de substanţe din jurul nostru. A fost nevoie totuşi de circa 50 de ani pentru ca ideea de atom să fie acceptată complet de comunitatea ştiinţifică. Aceasta s-a întâmplat în 1860, în timpului primului congres internaţional al chimiştilor, care de altfel a fost organizat tocmai pentru a dezbate chestiunea atomilor. Argumentul principal pentru existenţa atomilor era faptul că încă din 1850 se descoperise că aceştia au ceva în interiorul lor, o structură, pentru că din interior, ei emit... lumină. Se explicase astfel şi misterul originii luminii. Dar tot nu se cunoştea reţeta (legea, fenomenul) care făcea ca aceşti atomi să se combine pentru a crea molecule. Oamenii de ştiinţă trebuiau întâi să găsească cum pot fi aranjaţi aceşti atomi astfel încât să existe o regulă de grupare a lor.
A fost nevoie de nouă ani, pentru ca în 1869 răspunsul să vină de la chimistul rus Mendeleev, sub forma tabelului său periodic al elementelor chimice: atomii erau aranjaţi în ordinea crescătoare a masei lor şi rezulta că atomi aflaţi pe aceeaşi coloană aveau proprietăţi chimice similare. Era un punct de plecare spre descoperirea legii după care atomii se combinau în molecule.
Chimiştii au continuat efortul de a studia proprietăţile chimice ale fiecărui element chimic în parte, dar pasul decisiv a venit de la... fizică. În 1897, britanicul J. J. Thomson descoperea că toate tipurile de atomi studiate emiteau, în anumite condiţii, o radia-ţie de particule încărcate cu electricitate negativă. De aceea, au fost denumite electroni. Iată aşadar că atomii nu erau indivizibili, ci aveau o structură, care în jur de 1904 era înţeleasă astfel: tot aşa cum câteva stafide sunt răspândite într-un aluat continuu de chec, tot aşa şi electronii negativi erau răspândiţi într-un aluat încărcat electric pozitiv, astfel ca atomul per total să fie neutru. Pierderea unui electron transforma atomul într-un ion încercat pozitiv, iar acceptarea unui electron într-un ion încărcat negativ. Ionii pozitivi şi cei negativi se atrăgeau electric şi formau molecule stabile.
Iată deci cum în urmă cu aproape 100 de ani se cunoştea pentru prima dată reţeta Universului: forţa electrică era cea care ţinea ingredientele împreună, iar ingredientele erau câteva zeci de tipuri de atomi, combinaţi pentru a forma molecule, cristale şi toată diversitatea din viaţa noastră de zi cu zi. Dar despre cum a evoluat paradigma despre Univers vom afla mai multe în articolele viitoare.
Universul: reţetă şi ingrediente, partea a III-a
În primele două părţi am văzut împreună cum în Grecia Antică apa, aerul, pământul şi focul erau considerate ingredientele Universului şi cum despre reţeta după care se combinau ele nu se bănuia absolut nimic. Am văzut apoi cum ştiinţa modernă a arătat, în jur de anul 1770, că elementele acestea nu erau cu adevărat fundamentale, ci erau formate la rândul lor din elemente chimice. Am văzut cum în jur de 1810 s-a descoperit că fiecărui element chimic îi corespunde câte un tip de atom. Am aflat cum zeci de tipuri de atomi erau de fapt ingredientele Universului, iar reţeta după care aceştia se combinau în molecule era forţa electrică, căci atomii erau formaţi din electroni negativi răspândiţi într-o materie continuă pozitivă, precum stafidele sunt răspândite într-un cozonac. Pierzând sau captând electroni, atomii ce erau de obicei neutri din punct de vedere electric deveneau ioni încărcaţi electric, iar ionii pozitivi şi cei negativi se atrăgeau, creând o puzderie de tipuri de molecule, fără de care întregul Univers aşa cum îl ştim noi nu ar fi putut exista. Ştiinţa a oferit însă noi surprize şi s-a descoperit că nici atomii nu erau de fapt ingredientele fundamentale ale Universului, ci erau şi ei la rândul lor formaţi din alte componente mai mici. În acest articol vom explora împreună fascinanta poveste a descoperirii nucleului atomic.
S-a întâmplat în 1909 în cel mai bine dotat laborator din lume - la Universitatea Cambridge, Marea Britanie - sub comanda celui mai bun experimentator din lume: Ernest Rutherford. Rutheford dorea să testeze dacă modelul stafidelor din cozonac descria cu acurateţe atomul. Şi cum luase premiul Nobel cu doar un an înainte pentru studiul detaliat al unor radiaţii pe care le emiteau unii atomi, s-a folosit de acestea pentru a testa experimental modelul teoretic al atomului. Mai precis, a luat o foiţă de atomi de aur şi a bombardat-o cu aceste radiaţii. Modelul stafidelor din cozonac sugera că radiaţiile vor trece nedeviate prin foiţa de atomi de aur, sau că vor fi deviate foarte puţin. De notat că aceste radiaţii purtau numele de particule alfa şi Rutherford le înţelesese misterul pe vremea când era cercetător chiar în Montreal, la Universitatea McGill, cu câţiva ani mai înainte.
Tot aşa cum ai trage cu un glonţ printr-un zid de hârtie şi te-ai aştepta ca acesta să treacă nedeviat prin zid, Rutherford se aştepta ca particulele alfa să fie doar puţin deviate prin foiţa de atomi de aur. Nu mică i-a fost mirarea când a observat că de fapt cam una din opt mii de particule alfa revedea înapoi aproape complet. Era ca şi cum glonţul s-ar fi lovit de o zonă metalică ascunsă în zidul de hârtie! Şi atunci a înţeles: de fapt, atomul nu era plin, continuu, ca în modelul stafidelor din cozonac. Nu! Atomul era gol, cu un nucleu concentrat în centru, în jurul căruia electronii se roteau. Nucleul era foarte, foarte mic, iar atomul era mai ales gol. Aceasta era sugerat de faptul că doar una din opt mii de radiaţii alfa lovea un nucleu şi era deviată înapoi. Rutherford a măsurat precis raza nucleului: cam de o sută de mii de ori mai mică decât raza atomului. Imaginaţi-vă un stadion cu boabe de orez în partea superioară a tribunei, rotindu-se în jurul unui măr din centrul terenului şi veţi avea o imagine a atomului aproape la scară.
Rutherford a creat un nou model matematic al atomului în 1911 şi l-a denumit modelul planetar. Analogia între atom şi sistemul solar era evidentă. Aşa cum planetele se învârtesc în jurul Soarelui, tot astfel şi electronii orbitează la diferite distanţe în jurul nucleului; aşa cum Soarele conţine mai mult de 99% din masa întregului sistem solar, la fel şi nucleul conţine practic masa întregului atom; mai mult, precum există mult spaţiu gol în sistemul solar, tot aşa şi în atom există mult spaţiu gol.
Iată cum forţa electrică rămânea reţeta Universului, dar ingredientele sale fundamentale nu mai erau considerate zeci de tipuri de atomi, ci electroni şi zeci de tipuri de nuclee atomice. Despre cum a evoluat imaginea noastră despre cartea de bucate a Universului vom continua în articolul următor.
Universul: reţetă şi ingrediente, partea a IV-a
Iată-ne la a patra parte. Primul popas a fost în Grecia Antică de acum 2.500 de ani, când se credea că tot Universul este creat din patru ingrediente elementare (apă, aer, pământ şi foc) care sunt combinate după o reţetă necunoscută pentru a crea diversitatea din jurul nostru. Călătoria ne-a dus apoi pe urmele descoperirii elementelor chimice, atomilor şi apoi a nucleelor atomice. Şi am văzut cum din 1910 umanitatea ştia că de fapt ingredientele Universului sunt electronii şi câteva zeci de tipuri de nuclee. Electronii se roteau în jurul unui nucleu tot aşa cum planetele se rotesc în jurul unei stele. Reţeta Universului era aşadar forţa electrică, căci ea ţinea electronii în atomi şi atomii în molecule.

Descoperirile ştiinţifice s-au succedat apoi cu rapiditate, iar până în 1932 s-a cristalizat o nouă viziune asupra Universului.
În primul rând, fizicienii au rafinat modelul teoretic al atomului. Similitudinea între un sistem planetar şi un atom era de fapt imperfectă, căci dacă o planetă se poate deplasa în principiu la orice distanţă în jurul Soarelui, un electron se poate roti doar la distanţe precise în jurul unui nucleu. La fiecare astfel de distanţă precisă avea electronul o energie precisă. Saltul unui electron între aceste distanţe precise cu energii precise se făcea prin absorbţia sau emisia de energie sub formă de particule de lumină. Emisia şi absorbţia luminii, precum şi funcţionarea atomilor şi a moleculelor a fost explicată aşadar de fizică prin intermediul unei teorii fizice noi, revoluţionare, ce a apărut în anul 1925: mecanica cuantică. Reţeta care explica toate acestea (electricitate, magnetism şi lumină) era forţa electromagnetică.
În al doilea rând, la acelaşi laborator de la universitatea Cambridge din Marea Britanie şi acelaşi cercetător care a descoperit nucleul, Ernest Rutherford, a descoperit în 1919 şi ... protonul ca componentă a tuturor nucleelor din lume. Totodată, cel mai simplu nucleu existent era format dintr-un singur proton (nucleul de hidrogen). Protonul era pozitiv din punct de vedere electric.
Iar în 1932 tot la Cambridge a fost descoperit şi ... neutronul ca o componentă a tuturor nucleelor, mai puţin a celui de hidrogen. La început s-a crezut că de fapt neutronul ar fi un fel de atom format doar dintr-un proton şi electron, căci existau unele cazuri de dezintegrare nucleară când un neutron se transforma într-un proton şi electron. Dar noile legi ale mecanicii cuantice arătau că, în ciuda intuiţiei clasice, o particulă nu putea avea în acelaşi timp şi o poziţie fixă şi o viteză fixă. Astfel, dacă se ştia sigur ca electronul exista în interiorul nucleului, atunci rezulta ca electronul putea avea şi o viteză aşa de mare încât ar fi zburat din nucleu. Şi atunci nucleul nu mai fi fost stabil. Din fericire, după un deceniu de observaţii experimentale riguroase, James Chadwick a arătat că neutronul este de fapt o particulă de sine stătătoare, care nu conţine electronul în ea, ci care efectiv dispare şi lasă în urma sa un proton şi un electron atunci când are loc o dezintegrare nucleară.
Cu acestea, ingredientele Universului s-au simplificat uimitor. Dacă aţi fi un „bucătar cosmic”, nu ar trebui să aveţi în cămară zeci de tipuri de nuclee deja formate şi o cutie cu electroni. Ci ar fi suficient să aveţi o cutie cu protoni, o cutie cu neutroni şi una cu electroni! Explicarea Universului prin cât mai puţine ingrediente este unul din scopurile ştiinţei. Dar după ce reţetă trebuie puşi neutronii şi protonii pentru a sta împreună şi a crea nuclee stabile care să creeze atomi stabili şi să ne permită nouă să existăm? Dacă singura reţetă ar fi forţa electrică, protonii pozitivi s-ar respinge între ei, iar neutronii neutri nu ar participa la forţa electrică. Şi atunci cum de nucleul atomic este stabil? Dar despre aceasta în articolul următor ...
Universul: reţetă şi ingrediente, partea a V-a
Primii oameni care s-au întrebat din ce este format Universul şi care îi sunt legile după care elementele fundamentale se combină pentru a produce diversitatea din jurul nostru au fost filosofii din Grecia Antică, acum 2 milenii şi jumătate. Ei îşi imaginau că un „bucătar cosmic” ar trebui să aibă doar patru ingrediente: apă, aer, pământ şi foc. Dar nu ştiau reţeta după care aceste elemente trebuiau combinate pentru a produce plante, animale şi minerale. Două milenii şi jumătate mai târziu, în 1932, fizicienii ştiau că de fapt elementele grecilor sunt create la rândul lor din zeci de tipuri de atomi şi că toţi aceştia sunt formaţi doar din (alte) trei elemente: protoni, neutroni şi electroni. Dar care este reţeta misteriosului „bucătar cosmic”? Despre aceasta vom vorbi în continuare.

Reţeta Universului este formată de fapt din trei părţi. Fiecare parte corespunde unei forţe sau unei interacţiuni fundamentale între protoni, neutroni şi electroni. Căutând să înţelegem forţele fundamentale ale Universului, este important să subliniem cuvântul „fundamental”, care înseamnă că nu există o altă explicaţie care să includă o forţă mai profundă. De exemplu, în viaţa de zi cu zi simţim o mulţime de forţe diferite: forţa de frecare, care ne permite să mergem pe pământ şi maşinilor să înainteze - aţi văzut ce greu este să mergeţi pe gheaţă? fără frecare ar fi chiar imposibil; forţa de tensiune superficială - cea care permite apei să urce din sol în tulpinile copacilor sau cea care permite gâzelor să păşească pe suprafaţa apei fără să se scufunde; forţa elastică - cea care întinde un arc sau o praştie pentru vânătoare, sau care realizează suspensia la automobilul nostru; forţa de reacţiune normală - cea care nu ne lasă să cădem prin podea. Niciuna din aceste forţe nu este însă fundamentală. Fiecare este doar aspectul la scară mare a existenţei unei forţe la scară mică (atomică): este vorba despre forţa electrică.
Fiecare material este format din atomi, iar atomii sunt formaţi din nuclee pozitive şi electroni. Atomii din material interacţionează electric unii cu alţii şi, când se face suma forţei electrice, rezultă o forţă electrică totală care este percepută la nivel macroscopic ca şi forţă de frecare, sau forţă de tensiune superficială, sau forţă elastică, sau forţă de reacţiune normală. De exemplu, noi nu cădem prin podea pentru că atomii se atrag electric între ei şi nu vor să se despartă ca să formeze un hău prin care noi să cădem. Forţa electrică este cu mult mai puternică decât forţa gravitaţională: de miliarde de miliarde de miliarde de miliarde de ori mai tare (10^36)! Ce dovadă mai simplă decât faptul că întregul imens Pământ trage de un măr în jos şi noi putem contracara acea forţă cu doar două degete, prin forţa de frecare, adică prin atracţia electrică între atomii dintr-un deget cu cei din celalalt deget!
Forţa electrică este una din forţele fundamentale ale Universului. Povestea nu se termină însă aici, căci mai există o altă forţă, soră a ei: forţa magnetică. Ne este familiară de la magnetul pe care îl lipim pe frigider pentru a ţine o foiţă cu notiţe. Sau de la busola care ne arată nordul, deoarece întregul Pământ se comportă ca un magnet gigantic.
În anii 1700, când au fost studiate detaliat, se credea că este vorba de două forţe complet diferite, însă în 1820, danezul Orsted a făcut o descoperire surprinzătoare: un curent electric produce un câmp magnetic! Se descoperea astfel cum între cele două forţe există o legătură. A început atunci goana pentru demonstrarea fenomenul invers: poate un câmp magnetic genera curent electric? Răspunsul a fost da şi a venit în 1931 de la britanicul Faraday, moment din care ştim să producem curent electric alternativ în hidrocentrale, termocentrale sau centrale atomo-electrice. Iar în 1865, britanicul Maxwell a dezvoltat o teorie matematică care explica atât forţa electrică, cât şi cea magnetică, ca două aspecte diferite ale uneia şi aceleiaşi forţe fundamentale: forţa electromagnetică. Pentru prima dată, două forţe au fost unificate. Ce înseamnă unificate? În loc de două reţete ale Universului, era vorba doar de una. Ba chiar a existat şi o cireaşă pe tort, căci teoria lui Maxwell explica totodată şi misterioasa lumină: aceasta nu era altceva decât o undă electromagnetică. Electricitatea, magnetismul şi lumina erau aşadar descrise de una şi numai una din forţele fundamentale ale Universului, anume forţa electromagnetică. Ea este prima din cele trei părţi amintite din reţeta Universului. Despre celelalte două vom povesti în ediţiile viitoare.
Universul: reţetă şi ingrediente, partea a VI-a
În articolele precedente, fascinanta poveste a cunoaşterii Universului ne-a permis să călătorim din Grecia Antică a anului 500 î.e.n. până în Anglia anului 1932, când fizicienii au arătat că un ipotetic „bucătar cosmic” care ar dori să construiască toată materia din Univers nu ar avea nevoie decât de trei ingrediente de bază: protoni, neutroni şi electroni. Dar ce „carte de bucate” este necesară? Am discutat detaliat despre forţa electromagnetică, acea „reţetă” a Universului care ţine moleculele în substanţe, atomii în molecule şi electronii în atomi. Este forţa care stă la baza tuturor forţelor din viaţa de zi cu zi, precum forţa de frecare sau forţa elastică. Vom explora acum însă încă o forţă fundamentală a Universului.
Forţa electromagnetică ne este familiară din viaţa de zi cu zi, sub cele trei aspecte ale sale: forţa electrică, forţa magnetică şi lumina. Mai mult, toate forţele din viaţa de zi cu zi sunt de fapt manifestări la scară mare ale forţelor electrice dintre electronii atomilor din diferitele substanţe. Astfel, nu sunt forţe fundamentale forţa de frecare, forţa elastică, forţa de reacţiune normală sau forţa de tensiune superficială. De aceea nici nu le găsim în reţeta de bază a Universului. Acolo găsim însă forţa electromagnetică. Pe baza acestei reţete, folosind ca ingrediente electronii şi zeci de feluri de nuclee atomice, putem crea oricare din tipurile de atomi cunoscute, iar din acestea putem crea mii de molecule diferite, care pot crea sute de mii de substanţe diferite, adică toată diversitatea ce o vedem în jurul nostru.
Dar reţeta Universului nu este încă completă. Rămâne încă întrebarea: după ce reţetă sunt create zecile de tipuri de atomi plecând doar de la protoni şi neutroni ca ingrediente?
Haideţi să analizăm singura reţetă pe care o ştim deja: forţa electromagnetică. Poate ea ţine protoni şi neutroni împreună în nuclee? Aspectul forţei electromagnetice care are cea mai mică şansă să fie relevant aici este forţa electrică. Ori, din punct de vedere electric, un proton este pozitiv, iar un neutron este neutru. Mai ştim că două particule se resping prin forţă electrică dacă ambele sunt pozitive sau ambele negative şi se atrag dacă au semne diferite. Iar dacă una din particule are sarcină electrică zero, atunci forţa electrică nu se manifestă deloc. Cu acestea, putem aplica reţeta electrică asupra protonilor şi neutronilor strânşi la un loc: protonii se vor respinge cu alţi protoni; neutronii nici nu se vor respinge, nici nu se vor atrage cu alţi neutroni; iar protonii nici nu se vor respinge, nici nu se vor atrage cu alţi neutroni. Protonii şi neutronii sunt particule complet diferite din punctul de vedere al forţei electrice! Ei bine, rezultă că protonii s-ar respinge unii pe alţii, cu neutronii rămânând pasivi, şi atunci nucleul ar exploda, nu ar fi stabil şi atomii nu ar putea fi creaţi. Fără atomi, substanţele şi implicit noi, nu am exista. Trebuie atunci că mai există şi o altă reţetă a Universului, o altă forţă a naturii prin care protonii şi neutronii să se atragă. Mai mult, fiindcă forţa electrică de respingere există, trebuie ca această nouă forţă să fie mai puternică decât cea electrică.
Ei bine, această forţă chiar există şi poartă numele de forţă nucleară tare. I se spune „nucleară” pentru că explică cum pot exista nucleele. I se spune „tare” tocmai pentru că reuşeşte să contracareze forţa electrică. Conform acestei forţe, un proton şi un proton se atrag (deşi conform forţei electrice se resping!). Dar aceasta nu este tot! Conform aceleaşi forţe tari, şi un neutron şi un neutron se atrag! Ba mai mult, şi un proton şi un neutron se atrag! Şi cum protonul şi neutronul au o masă foarte apropiată, în toate cazurile de mai sus forţa are aceeaşi tărie. Aşadar, pentru forţa nucleară tare protonul şi neutronul sunt de fapt una şi aceeaşi particulă, cunoscută sub numele de nucleon. Şi oricare doi nucleoni se atrag reciproc.
Dar ... există un dar. Dacă un proton şi un electron se atrag electric la orice distanţă s-ar afla, doi nucleoni nu se atrag decât dacă se află la distanţe foarte mici, de aproximativ lungimea a câţiva protoni sau neutroni puşi cap la cap. Cu alte cuvinte, pentru a forma nuclee este necesar să se consume o cantitate de obicei foarte mare de energie pentru a învinge forţa electrică dintre protoni şi a-i apropia. Dar odată apropiaţi, dacă în acelaşi loc ajung şi neutroni, atunci neutronii şi protonii încep să se atragă şi să formeze nuclee stabile. Aceste condiţii speciale de temperaturi şi presiuni uriaşe se realizează într-un loc special în Univers, un loc fără de care noi nu am exista, căci nucleele nu s-ar fi format. Este vorba de stele... Nucleele atomice au fost create într-adevăr în stele şi noi existăm pentru că înaintea Soarelui nostru alte stele au trăit şi au murit. Iar reţeta Universului datorită căreia nucleele atomice există este forţa nucleară tare. Dar explicarea Universului nu s-a terminat şi mai există o reţetă a Universului, pe care vom explora în numărul viitor.
Universul: reţetă şi ingrediente, partea a VII-a
În această parte explic forţa nucleara slabă, cea care face din visul alchimiştilor o realitate (transformarea elementelor chimice din unul în altul) şi fără de care Soarele nostru nu ar arde şi noi nu am exista.

Forţa nucleară slabă permite atomilor să se schimbe dintr-un tip într-altul, exact ca în visul alchimiştilor din Antichitate.
Dacă am dori să recreăm Universul nostru de la zero, cum am face-o? Care îi sunt ingredientele şi care îi este reţeta? În cele şase articole precedente am călătorit, odată cu omenirea, de la credinţa din Grecia Antică în patru elemente fundamentale, unite de o reţetă misterioasă pentru a crea diversitatea din jurul nostru, până la anul de cotitură 1932, când a fost descoperit neutronul. Cu această descoperire, ultima bucăţică de puzzle al reţetei Universului a fost pusă la locul ei, iar imaginea despre Univers s-a completat. Ingredientele sale de bază erau aşadar doar trei: protoni, neutroni şi electroni. Iar reţeta după care acestea se combinau erau tot trei: forţa electromagnetică – care ţine moleculele în substanţe, atomii în molecule şi nucleele şi electronii în atomi; forţa nucleară tare – care ţine protonii şi neutronii în nuclee; forţa nucleară slabă - care permite atomilor să se schimbe dintr-un tip într-altul, exact ca în visul alchimiştilor din Antichitate. Dacă în articolele precedente am explorat în detaliu forţa electromagnetică şi forţa nucleară tare, astăzi vom povesti despre forţa nucleară slabă.
Dacă atomii nu ar exista, nici noi nu am exista. Şi nu doar noi, ci nici planetele, stelele sau praful interstelar. Iar atomii nu ar exista dacă această diversitate de zeci de tipuri de nuclee nu ar exista.
Imediat după Big Bang au luat fiinţă doar cele mai uşoare tipuri de atomi: hidrogenul (cu nucleul format dintr-un proton), heliul (cu nucleul format din doi protoni şi doi neutroni) şi foarte mici cantităţi de litiu. Toate celelalte elemente chimice au fost create în stele.
Primele stele erau mari aglomerări de hidrogen şi heliu. Cu cât mai mari, cu atât era mai intensă gravitaţia în centrul norului gazos, şi cu atât mai mari presiunea şi temperatura. Dincolo de un anume punct, începeau să aibă loc reacţii termo-nucleare. Cu alte cuvinte, patru nuclee de hidrogen se transformau într-un nucleu de heliu. Era aşadar o reacţie nucleară, însă în urma ei era produsă energie, de unde termenul de termo. Această energie menţine steaua fierbinte, generând ca reacţia termonucleară să se autosusţină până când hidrogenul din stele se transformă aproape în totalitate în heliu. Tot această energie este emanată de stea sub formă de lumină. Cum aproape toată viaţa de pe Pământ îşi ia energia de la Soare, putem spune că la baza vieţii noastre sunt reacţiile termonucleare din Soare. Ceea ce ţine cei doi protoni şi doi neutroni din heliu împreună, luptând contra forţei electrice care vrea să explodeze nucleul (deoarece electric cei doi protoni se resping iar neutronii nu au o forţă electrică), este forţa nucleară tare, pentru care protonul şi neutronul sunt una şi aceeaşi particulă (denumită generic nucleon) şi oricare doi nucleoni se atrag, ba încă şi mai intens decât forţa electrică, de unde şi denumirea de forţa nucleară tare.
Dar ... există şi aici un dar. Dacă plecăm de la patru atomi de hidrogen şi ajungem la unul de heliu, înseamnă că plecăm de la patru protoni şi ajungem la doi protoni şi doi neutroni. Cum este posibil aceasta? Ei bine, tocmai aici intervine cea de-a treia forţa fundamentală a Universului, anume forţa nucleară slabă. Ea este cea care permite în anumite condiţii unui proton să se transforme într-un neutron, iar unui neutron să se transforme într-un proton. I se spune „nucleară”, căci schimbându-se structura nucleelor, se schimbă practic elementul chimic (ori acesta este exact visul celebru al alchimiştilor antici, vis pe care ştiinţa modernă l-a făcut realitate). I se spune „slabă” pentru că numai în anumite condiţii şi numai foarte rar are loc această transformare. Altfel, atomii s-ar schimba prea des între ei şi lumea ar fi prea instabilă. Dar exact atunci când trebuie, apare forţa nucleară slabă şi permite stelelor să ardă, oferindu-ne nouă energia de care avem nevoie.
Şi mai este un aspect: interiorul Pământului este fierbinte (şi putem lua energie geotermală, de exemplu) pentru că în interiorul Pământului există anumiţi atomi (de uraniu) a căror neutroni se transformă în protoni emiţând energie (acest proces se numeşte dezintegrare nucleară sau radioactivitate). Iar această energie încălzeşte interiorul Pământului, oferind energie pentru bacteriile ce trăiesc fără lumină solară sau nouă oferindu-ne energie geotermală.
Universul: reţetă şi ingrediente, partea a VIII-a
În această parte a articolului introduc pe înţelesul tuturor ideea de antimaterie, despre care vom povesti şi în următoarele două părţi.

Cantitatea de radiaţie scade pe măsură ce ne ridicăm de la sol, până la 1-2 kilometri. Apoi începe iarăşi să crească pe măsură ce creşte altitudinea, datorită radiaţiei care vine din spaţiul cosmic şi loveşte atmosfera Pământului. Radiaţia cosmică a fost descoperită de Victor Hess în 1912.
Introducere
În cele şapte părţi precedente am explorat răspunsurile umanităţii de-a lungul mileniilor la întrebarea profundă din ce suntem formaţi, atât noi ca materie vie, cât şi ceea ce ne înconjoară ca materie nevie. Am văzut cum în Grecia Antică se credea că ingredientele fundamentale ale Universului sunt apa, aerul, pământul şi focul, dar cum în ultimii 250 de ani ştiinţa modernă a înţeles că acestea sunt de fapt elemente chimice, care sunt formate din atomi, care sunt formaţi din protoni, neutroni şi electroni. Am văzut cum grecii antici nu aveau nici cea mai mică idee despre reţeta după care cele patru elemente fundamentale se combină, dar cum ştiinţa modernă a arătat că reţeta Universului este formată din trei forţe fundamentale, care ţin protonii, neutronii şi electronii împreună: forţa electromagnetică, forţa nucleară tare şi forţa nucleară slabă. În fascinanta noastră călătorie, am ajuns aşadar la borna kilometrică a anului 1932. Oamenii de ştiinţă credeau atunci că au înţeles cu totul Universul şi chiar regretau că nu mai au ce descoperiri noi să facă în fizică. Nu mare le-a fost mirarea când imediat după a fost descoperită o nouă particulă subatomică, un nou ingredient al Universului, despre care nu se ştia însă ce rol ar putea juca în reţeta Universului. Vom vorbi în acest articol despre una din aceste descoperiri surprinzătoare: radiaţiile cosmice, care au dus apoi la descoperirea ... antimateriei şi nu numai.
1896: descoperirea radioactivităţii
Pentru aceasta, trebuie să ne întoarcem puţin în timp. În 1896 a fost descoperit de fizicianul francez Becquerel un fenomen prin care anumite elemente chimice, precum uraniul, emit radiaţii, adică particule subatomice aruncate cu viteză mare din interiorul atomului. Fenomenul a fost apoi studiat detaliat de soţii Curie tot în Franţa, care au descoperit, cam prin anul 1902, noi elemente chimice radioactive. Imediat a început să studieze detaliat radioactivitatea şi fizicianul englez Ernest Rutherford, când a fost trimis la universitatea McGill din Montreal, pentru a pune pe picioare un departament serios de fizică şi în Canada. În acei câţiva ani la McGill, Rutherford a înţeles că particulele emise sunt de trei tipuri: radiaţii alfa (nuclee de heliu, adică formate din doi protoni şi doi neutroni), radiaţii beta (electroni) şi radiaţii gama (fotoni, adică particule de lumină). Pentru aceasta a luat premiul Nobel pentru Chimie în 1907. După ce s-a întors în Anglia, a folosit radiaţiile alfa pentru a bombarda o foiţă de atomi de aur, iar cu aceasta a descoperit în 1910, acum o sută de ani, nucleul atomului.
1912: descoperirea radiaţiilor cosmice
Ajungem aşadar în anul 1912. Atunci se ştia că şi solul are o radioactivitate naturală, pentru că în sol sunt cantităţi foarte mici, dar măsurabile, de uraniu şi alte elemente chimice radioactive. Se construiseră deja detectoare performante de radiaţie şi părea evident că pe măsură ce te ridici la o înălţime mai mare, cantitatea de radiaţie provenită de la sol trebuie să scadă. Ei bine, chiar asta şi-a propus să verifice experimental fizicianul austriac Victor Hess în 1912. La început a realizat experimentul în turnul Eiffel din Paris, pe atunci cea mai înaltă construcţie din lume. Pentru a studia fenomenul la înălţimi şi mai mari, Hess a aranjat să zboare cu un balon până la 5.000 de metri. A realizat măsurători atât ziua cât şi noaptea, pentru a avea toate datele disponibile. La sfârşit, a arătat lumii o mare descoperire: cantitatea de radiaţie scade într-adevăr pe măsură ce ne ridicăm de la sol şi face aşa timp de cam 1-2 kilometri. Dar apoi, surprinzător, începe iarăşi să crească. Şi creşte încontinuu pe măsură ce creşte altitudinea. Există o singură explicaţie, a conchis Hess: există radiaţie care vine din spaţiul cosmic şi loveşte atmosfera Pământului. Victor Hess descoperise aşadar radiaţiile cosmice.
1932: descoperirea antimateriei
Descoperirea sa a fost reprodusă cu succes de fizicianul american Robert Millikan în 1925. Imediat acesta a creat un program intens de cercetare a radiaţiilor cosmice la universitatea Caltech, în California, unde, în 1932, studentul său Carl Anderson a descoperit în radiaţiile cosmice un nou ingredient fundamental al Universului, un frate geamăn al electronului, anume particula de antimaterie corespunzătoare electronului. Este vorba de o particulă cu toate proprietăţile electronului, numai că în loc să fie negativ din punct de vedere electric, este pozitiv. I s-a dat numele de antielectron sau pozitron.
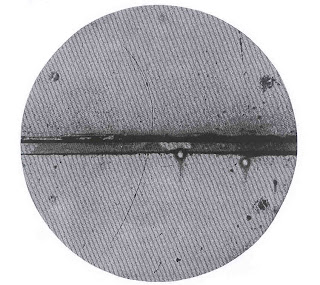
În1932, în radiaţia cosmică, a fost descoperit un nou ingredient fundamental al Universului, pozitronul, o particulă de antimaterie corespunzătoare electronului. El este fratele geamăn al electronului, numai că loc să fie negativ din punct de vedere electric, este pozitiv.
1936: Premiul Nobel pentru radiaţii cosmice şi antimaterie
Descoperirea antimateriei a fost foarte profundă şi un şoc pentru fizica modernă exact în anul 1932, când se credea că totul fusese înţeles odată cu identificarea neutronului. Şi cum descoperirea antimateriei nu ar fi fost posibilă fără descoperirea radiaţiilor cosmice, premiul Nobel pentru fizică a fost acordat în 1936 cercetătorilor Victor Hess şi Carl Anderson.
Despre antimaterie vom vorbi mai pe larg în articolele următoare. La fel, vom afla că şi alte particule elementare surprinzătoare au fost descoperite tot în radiaţiile cosmice.
Universul: reţetă şi ingrediente, partea a IX-a
În 1932, fizicienii credeau că înţeleseseră misterele materiei. Ei realizaseră că ingredientele fundamentale ale Universului sunt protonii, neutronii şi electronii şi că reţeta după care acestea se combină pentru a produce diversitatea materiei din jurul nostru se constituie din trei forţe elementare: forţa electromagnetică, forţa nucleară tare şi forţa nucleară slabă. În articolul precedent am văzut cum fizicienii au avut însă, tot în 1932, o surpriză de proporţii: pentru fiecare ingredient fundamental al Universului există încă unul geamăn, care are aceeaşi masă, dar sarcină electrică de semn opus. Este vorba de antimaterie.

Antimaterie: pentru fiecare ingredient fundamental al Universului există încă unul geamăn, care are aceeaşi masă, dar sarcină electrică de semn opus.
Antimateria nu este un subiect de science-fiction, ci este o componentă reală a Universului nostru, descoperită experimental acum 78 de ani. Cu patru ani mai înainte însă, în 1928, o teorie revoluţionară a fizicii de la acea vreme prezisese existenţa antimateriei fără ca nimeni - nici măcar autorul ei - să-şi fi dat seama de aceasta. Pentru a înţelege despre ce este vorba, vom coborî şi mai înainte în timp.
Teoria care explică legile după care un electron se mişcă sub acţiunea unei forţe electrice, după care lumina este emisă sau absorbită de atomi, după care un magnet interacţionează cu un alt magnet, poartă numele de teoria electromagnetică. A fost creată în 1865 de fizicianul britanic James Clark Maxwell, unificând electricitatea şi magnetismul într-o singură teorie. Mai mult, ea a prezis existenţa unor unde electromagnetice, care se deplasau cu o viteză ce depinde de constantele vidului pentru electricitate şi magnetism. Formula respectivă reieşea din teoria lui Maxwell iar când acesta a introdus valorile măsurate în formulă, stupoarea a fost uriaşă. Viteza undelor electromagnetice era egală cu viteza deja măsurată a luminii în vid!
Reflectând la această coincidenţă, Maxwell a înţeles că de fapt nu este vorba de o coincidenţă. Emisia şi absorbţia luminii erau legate de electricitate şi magnetism. Se ştia deja, încă de la 1850, că lumina este emisă şi absorbită de atomi. Maxwell a arătat că un electron, atunci când este accelerat sau frânat, emite lumină. Iată aşadar cum în 1865 omenirea a produs prima teorie care unifica trei fenomene ce se considerau complet diferite: electricitatea, magnetismul şi lumina.
Detaliile despre emisia şi absorbţia luminii în atomi au fost explicate teoretic în anul 1925, atunci când aproape din senin s-a dezvoltat o teorie matematică care arăta precis frecvenţele de lumină emise sau absorbite de diferiţi atomi. Este vorba de teoria cuantică. Aceasta explica faptul că în atomi electronii sunt aşezaţi pe diferite straturi energetice (în 1865, Maxwell ştia că există atomi, dar nu ştia că există electroni şi nu ştia nimic despre structura atomilor). Când un electron trece de la un nivel de energie la un altul în interiorul atomului, atunci trece şi de la o anumită viteză la alta, fiind astfel accelerat sau frânat. Ori, Mawell explicase că atunci când un electron este accelerat sau frânat el emite lumină. Frecvenţa luminii emise era dată de diferenţa de energie între nivelul iniţial şi cel final al electronului în atomi. Iar aceste nivele energetice ale unui atom dat puteau fi calculate precis plecând de la ecuaţia lui Schrodinger, care era de fapt ecuaţia lui Mawell „cuantificată”. Cuantificarea este un procedeu matematic prin care se trece de la legile clasice din viaţa de zi cu zi la legile din lumea atomică, legi ce sunt contraintuitive şi diferite de cele ale materiei la scară mare.
Iată aşadar cum mecanica cuantică explica în 1925 descoperirea lui Maxwell: lumina este legată de electron prin proprietăţile lui electrice. Dar are electronul şi proprietăţi magnetice? În 1922 fusese descoperit, experimental într-adevăr, că electronul chiar şi în afara atomului, singur, se comportă ca un mic magnet. O teorie a electronului care să ia în calcul magnetismul său intrinsec (denumit spin) a fost dezvoltată în 1928 de către matematicianul britanic Adrien Paul Maurice Dirac. Şi tocmai această teorie a prezis existenţa antimateriei, fără ca măcar Dirac să bănuiască. Mai multe despre aceasta în episodul următor.

Teoria cuantică explica în 1925 faptul că în atomi electronii sunt aşezaţi pe diferite starturi energetice.
Universul: reţetă şi ingrediente, partea a X-a
În ultimele două episoade am discutat despre antimaterie. Am arătat cum în mod surprinzător, în 1932, ea fost descoperită experimental în radiaţii cosmice, sub forma unui electron de aceeaşi masă cu electronul obişnuit, dar cu sarcină electrică de semn opus. Am arătat cum în 1928 a apărut o teorie care a prezis antimateria, fără însă ca autorul ei să îşi fi dat seama. Am arătat, de asemenea, evoluţia teoriilor fizice de la 1865 (teoria electromagnetică) la 1925 (teoria cuantică) pentru a explica electricitatea, magnetismul şi lumina. Vom continua expunerea...

În 1928, fizicianul britanic Paul Adrien Maurice Dirac a explicat cum se deplasează prin spaţiu un electron ce are sarcină electrică (adică are proprietăţi electrice) şi spin (adică are proprietăţi magnetice).
Întâi, să ne mai întoarcem puţin în timp faţă de anul 1925, cel al teoriei cuantice. În 1922, doi fizicieni germani, Stern şi Gerlach, au realizat un experiment prin care au arătat că electronul se comportă ca un... mic magnet! Se ştia deja că atunci când orbitează în jurul nucleului, electronul reprezintă o mişcare de sarcină electrică, ceea ce reprezintă un curent electric. Cum orice curent electric creează un câmp magnetic, mişcându-se într-un atom, electronul formează un mic magnet. De altfel, aşa se şi face că diferite materiale sunt magnetice. Lucrul aceste se ştia deja de un secol, însă ceea ce Stern şi Gerlach au arătat este că electronul, chiar şi atunci când nu se află într-un atom, ci liber, deplasându-se cu viteză constantă, este totuşi un mic magnet. Ca şi cum electronul s-ar învârti în jurul propriei axe, deşi este un punct şi nu are o axă. Această proprietate cuantică a electronului a fost denumită spin, de la englezescul „to spin”, adică „a se roti”.
Ecuaţia lui Schordinger nu lua însă în considerare şi nici nu explica spinul electronului. Cel care a reuşit să dezvolte pentru prima dată o teorie cuantică a electronului care să includă şi spinul său a fost fizicianul britanic Paul Adrien Maurice Dirac, în 1928. Teoria sa a fost una revoluţionară, care a venit la doar trei ani de la o altă teorie revoluţionară, mecanica cuantică, pe care a extins-o şi a dus-o mai departe. Dirac a explicat cum există sau cum se deplasează prin spaţiu un electron ce are sarcină electrică (adică are proprietăţi electrice) şi spin (adică are proprietăţi magnetice).
Dar cum prezicea această teorie în mod subtil existenţa antimateriei? Să vedem o analogie. Dacă vi se cere un număr care ridicat la pătrat este 9, veţi spune că numărul căutat este 3. Un matematician v-ar răspunde că ar mai exista o soluţie, anume minus 3. Dumneavoastră i-aţi răspunde că are dreptate, dar că din păcate pentru el ştiţi din surse sigure că numărul căutat e musai pozitiv, ca de exemplu energia de mişcare a unui corp. Energia de mişcare este de forma ½ ori masa ori viteza la pătrat. Şi cum masa este mereu pozitivă, energia de mişcare este pozitivă. Şi atunci procedaţi aşa cum aţi fost învăţaţi la fizică în liceu: aruncaţi soluţia negativă ca neavând semnificaţie fizică. Ei bine, aşa a făcut şi Dirac când noua sa ecuaţie spunea că energia la pătrat are o anumită valoare pozitivă. Era evident că energia ar fi radical din acea valoare. De ce ar trebui ca energia să poată fi şi minus radical din acea valoare? O energie de mişcare negativă nu are sens, decât dacă cumva ar fi vorba de masă negativă. Iar o masă negativă nu are sens, pentru că forţa gravitaţională este doar de atracţie. La forţa electrică există şi sarcini negative pe lângă cele pozitive pentru că forţa electrică poate fi şi repulsivă, nu doar atractivă. Dar forţa gravitaţională este doar atractivă şi atunci masa e doar pozitivă. Nu e aşadar de mirare că Dirac a aruncat această soluţie imediat ce a văzut-o matematic, căci nu avea suport fizic.
Descoperirea experimentală a antimateriei în 1932 l-a îndemnat să se mai uite odată la ecuaţiile sale. Antielectronul observat de Carl Anderson în radiaţiile cosmice era un electron de aceeaşi masă, numai că avea sarcină electrică de semn opus. Dirac şi-a dat seama că matematic acel semn minus de la a doua soluţie din ecuaţie putea fi interpretat nu doar ca o masă negativă, ci şi ca un mers negativ în timp (adică mers spre trecut) sau mers negativ în spaţiu (adică mers în sens opus decât ar merge un electron cu aceeaşi energie). Dar nici acestea nu aveau sens. Sau se mai putea (şi de aici a licărit speranţa!) ca acel semn minus să fie interpretat ca un semn minus la sarcina electrică. Adică un electron cu aceeaşi masă ca şi electronul, dar cu semn electric pozitiv. Şi tocmai aceasta, un antielectron, denumit apoi şi pozitron, descoperise Andersen.
Iată aşadar cum ingredientele Universului trebuie înmulţite cu doi, pentru că şi protonul şi neutronul au partenerii lor de antimaterie (antiprotonul şi antineutronul), chiar dacă au fost descoperiţi experimental ceva mai târziu.
Universul: reţetă şi ingrediente, partea a XI-a
După 10 părţi de introducere în fizica subatomică, a venit rândul să discutăm despre o nouă particulă elementară, frate al electronului: muonul sau particula mu. Iar o coincidenţă fericită ne aduce chiar o ştire mare din fizica particulelor, apărută pe coperta ultimului număr din prestigioasa revistă Nature. Muonul a ajutat la măsurarea precisă a razei protonului şi spre surpriza tuturor, valoarea obţinută este cu 4% mai mică decât valoarea oficială. Aceasta are implicaţii imense asupra înţelegerii noastre a Universului mic, care va trebui ajustat corespunzător.
Protonii, unele din părţile componente ale atomului, sunt mai mici decât se credea - o descoperire surprinzătoare care poate altera cele mai de încredere legi ale fizicii.
Din această serie de articole de istoria ştiinţei suntem deja familiari cu ideea că totul în jurul nostru este format din atomi, care sunt formaţi din câte un nucleu în jurul căruia se învârt electroni. Nucleele sunt formate la rândul lor din protoni şi neutroni. Aşadar, nucleele nu sunt punctiforme, ci au o rază şi un volum. Dar nici protonii şi neutronii nu sunt punctiformi, ci au o rază şi un volum. Aceasta pentru că fiecare din ei are o structură. Sunt constituiţi din câte trei particule elementare denumite cuarci care schimbă între ei alte particule denumite gluoni. Protonul are, prin urmare, o rază care este dată de structura sa şi de mişcările particulelor elementare din interiorul său. Un proton singur reprezintă şi cel mai mic nucleu de atom din natură. Este chiar nucleul de hidrogen, căci un proton în jurul căruia se învârte un electron formează atomul de hidrogen. Spre deosebire de majoritatea atomilor care sunt creaţi în stele care transformă hidrogen şi heliu în atomi mai grei, atomii de hidrogen au fost creaţi chiar imediat după Big Bang prin acelaşi mecanism din care s-a format Universul nostru.
În ceea ce priveşte electronul, acesta nu are o structură, ci este o particulă elementară, cu rază zero şi volum zero.
Raza protonului a fost măsurată acum aproximativ 40 de ani şi de atunci nu s-au mai făcut alte măsurători. Dar iată că un experiment nou, de zece ori mai precis, a fost finalizat recent, după doisprezece ani de muncă, între care şase doar de verificare a rezultatului incredibil observat: raza protonului este cu 4 procente mai mică decât valoarea măsurată în trecut. În condiţiile în care teoriile fizicii particulelor elementare sunt precise la a treia zecimală, o diferenţă la zecimala a doua este şocantă şi retrimite fizicienii, atât pe teoreticieni, cât şi pe experimentatori, la foaia de hârtie, respectiv la acceleratoarele de particule.
CE ESTE MUONUL?
Muonul este o altă particulă elementară. Este de fapt tot un fel de electron, numai că de aproape 200 de ori mai masiv. Are tot sarcină electrică negativă şi tot rază şi volum zero. Dar dacă un electron este stabil, adică trăieşte la infinit, un muon „moare” după cam 2 milionimi de secundă, dispărând şi lăsând în locul său un electron şi doi neutrino, particule de care vom vorbi în articolele viitoare. E suficient să înţelegem că un muon este un electron mai masiv, instabil, care se dezintegrează într-un electron şi alte particule după un timp foarte scurt pentru ochii noştri, dar foarte mare pentru lumea subatomică.
Atât de mare, încât fizicienii au reuşit să creeze cu ajutorul unui accelerator de particule de la Institutul Paul Scherrer din Elveţia (CERN nu are singurul accelerator de particule din Elveţia!) un fascicul de muoni cu care au bombardat un recipient ce conţinea atomi de hidrogen. Câteodată un muon disocia o moleculă de hidrogen în doi atomi de hidrogen, unuia dintre aceştia trimiţându-i electronul în afară, pentru ca locul său să fie luat chiar de muon!
Cum muonul este tot un fel de electron, numai că mai masiv şi care trăieşte mai puţin, iată că se poate crea un nou tip de atom: un hidrogen muonic, unde în jurul protonului se învârte un muon, nu un electron. Dacă atomul cu electron trăieşte la infinit, atomul cu muon trăieşte doar vreo două milionimi de secundă. Cum acesta este un interval de timp mare pentru lumea subatomică, fizicienii au putut studia interacţia dintre proton şi muon. Fiind cam 200 de ori mai masiv ca electronul, muonul este mult mai aproape de proton decât ar fi electronul, iar acest lucru a permis măsurarea razei protonului mult mai precis ca până acum. Rezultatul surprinzător că de fapt raza protonului era supradimensionată cu 4% cere fizicienilor să revizuiască parametrii teoriei fizicii particulelor şi apoi predicţiile pe care aceasta le face. Va influenţa acest rezultat experimentele de la acceleratorul LHC? Rămâne de văzut continuarea acestei poveşti.
Articol scris de Adrian Buzatu pentru revista Accent Montreal.
